Dr. Paola Antonini, direttore scientifico Meditrial.
Se ben progettati, studi osservazionali e registri producono dati sull’effetto del trattamento paragonabili per importanza a quelli degli studi randomizzati controllati[1] , generando informazioni mancanti negli studi interventistici tradizionali e dati dal mondo reale a supporto dell’autorizzazione all’immissione in commercio.
Quale disegno?
Gli studi osservazionali offrono un continuum di disegni descrittivi, esplorativi e sperimentali.
Questi includono case study, studi trasversali, studi caso-controllo, disegni retrospettivi, studi di coorte longitudinali, studi caso-controllo nested [2]. I registri dei pazienti sono una componente importante all’interno di questo armamentario in quanto facilitano l’acquisizione di dati di efficacia e sicurezza a lungo termine e forniscono informazioni sulla penetrazione nel mercato e sulle abitudini di prescrizione di farmaci, biologici o dispositivi di nuova introduzione[3].
Inoltre, i registri e altre forme di ricerca osservazionale consentono di concentrarsi sui risultati riportati dai pazienti, catturando così una prospettiva a 360° sull’efficacia dei farmaci e dei dispositivi e sul miglioramento della qualità di vita. Grazie all’inclusione di pazienti con malattie e terapie concomitanti, i dati osservazionali facilitano l’esame di sottogruppi che in precedenza potevano non essere stati individuati, nei quali il rapporto beneficio/rischio viene migliorato e per i quali sono giustificate ulteriori indagini in contesti ben controllati, ad esempio utilizzando variabili fenotipiche/genotipiche che impattino sulla risposta al trattamento[4].
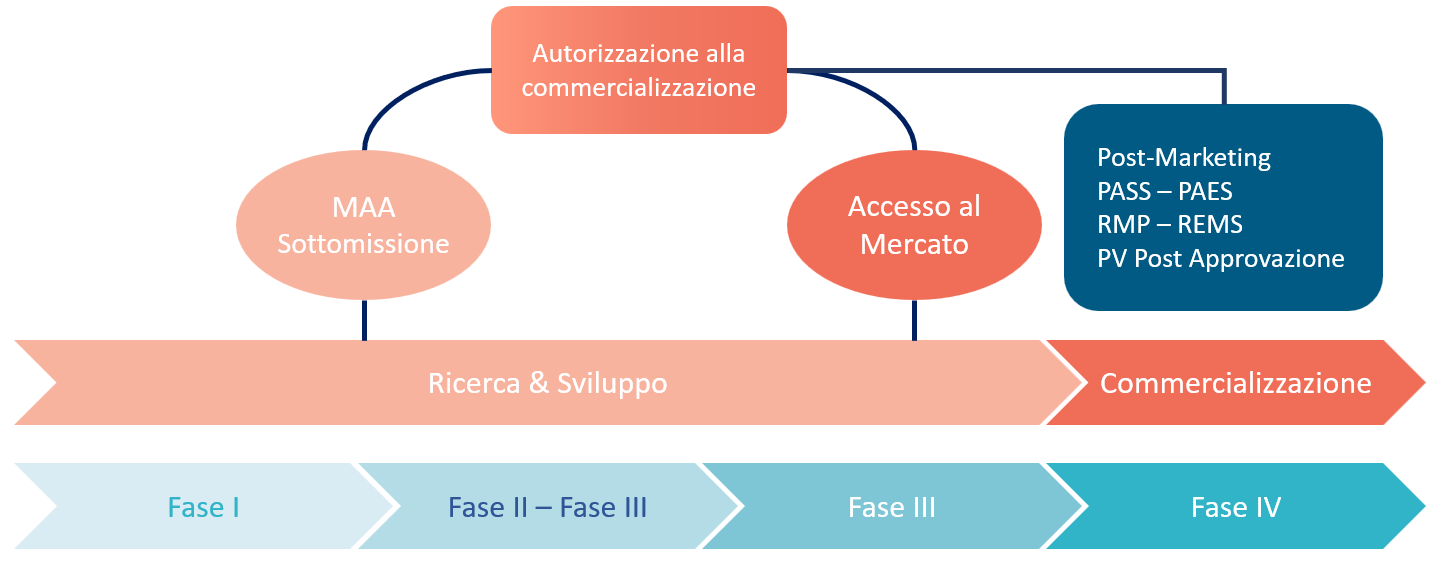
Per la natura stessa della popolazione valutata, i registri facilitano in particolare l’identificazione dell’uso off label in indicazioni potenzialmente nuove, consentono il monitoraggio della sicurezza a lungo termine e forniscono informazioni sulle stime della comorbidità e dell’uso concomitante di altri farmaci[5]. La progettazione degli studi e il tipo di dati raccolti variano in base all’uso finale previsto delle informazioni.
Molteplicità degli stakeholder
Il mix di studi interventistici e osservazionali in un programma di sviluppo si riflette nel mix di stakeholder coinvolti in questo processo.
Per esempio, i pazienti potrebbero essere specificamente interessati ai risultati direttamente correlati al sintomo più preoccupante della malattia laddove i payers si concentrano maggiormente sulla copertura e determinazione dei prezzi. In effetti, in un programma di sviluppo clinico che deve includere studi che coprano l’intero ciclo di vita del farmaco, la pianificazione degli studi osservazionali, compresi i registri, avviene nella fase pre-registrativa, quando le principali caratteristiche del prodotto sono già delineate ma necessitano di essere ulteriormente definite.
Progettare il successo
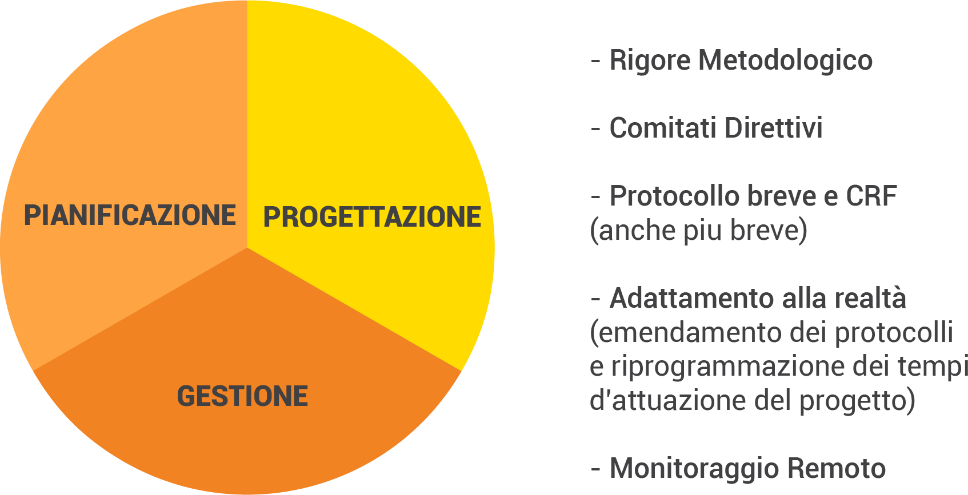 I progetti di ricerca osservazionale includono diverse tipologie di studi diversamente denominati, quali studi non interventistici (NIS, not interventional studies), programmi per uso compassionevole, registri, studi post-autorizzazione di sicurezza o efficacia (PASS o PAES), programmi di expanded access, studi di fase IIIB/IV.
I progetti di ricerca osservazionale includono diverse tipologie di studi diversamente denominati, quali studi non interventistici (NIS, not interventional studies), programmi per uso compassionevole, registri, studi post-autorizzazione di sicurezza o efficacia (PASS o PAES), programmi di expanded access, studi di fase IIIB/IV.
Tali progetti di ricerca necessitano di una solida metodologia, di comitati direttivi e di varie permutazioni di monitoraggio remoto. Protocolli brevi (e anche case report form che siano snelle nella struttura) facilitano la partecipazione di medici che hanno talvolta poca familiarità con i requisiti della ricerca clinica. Infine, la conoscenza delle tempistiche di registrazione è essenziale per ottimizzare i tempi di studio.
In un progetto di ricerca osservazionale vi possono essere vantaggi bidirezionali nella collaborazione tra aziende sponsor e CRO, ai fini della selezione accurata dei centri, della gestione adeguata di un avvio non uniforme di molteplici siti nei differenti Paesi coinvolti e dell’aderenza alle varie normative.
TAKE HOME MESSAGES
- Gli studi osservazionali sono atti a valutare gli effetti di interazione
Una volta superato il contesto registrativo o di approvazione, farmaci, prodotti biologici e i dispositivi entrano nella complessa matrice di gestione clinica del paziente sottoposto a molteplici interventi terapeutici che rappresentano gli standard di cura in assenza del nuovo intervento. L’interazione tra trattamenti consolidati con il più recente “strumento terapeutico” crea uno quadro di complessità che necessita nuove evidenze. Queste nuove evidenze vengono fornite dai programmi osservazionali.
- L’importanza di includere gli studi osservazionali nel portfolio di studi clinici che iniziano con i first-in-human
Gli studi osservazionali, inclusi i registri, sono all’interno di un portfolio di studi clinici atti a produrre la varietà di dati utilizzati nei processi decisionali per il posizionamento nel prontuario, il rimborso e l’accesso del paziente a farmaci, prodotti biologici o dispositivi. I dati pubblicati di tali studi clinici sono apprezzati da un pubblico esperto, quantificano l’impatto sul sistema sanitario e facilitano il processo decisionale di un insieme sempre più eterogeneo di stakeholder, ognuno con richieste specifiche di dati.
A cura di Paola Antonini, direttore scientifico Meditrial
[1] 1. FConcato J, Shah N, Horwitz RI. Randomized, controlled trials, observational studies, and the hierarchy of research designs. N Engl J Med. 2000 Jun 22;342(25):1887-92.
[2] Shah, N. Evidence standards in the era of comparative effectiveness. AHDB.2(1): s41-s48, 2009.
[3] 4. Polygenis D, ed. ISPOR Taxonomy of Patient Registries: Classification, Characteristics and Terms. Lawrenceville, NJ; 2013.
[4] Murphy M. Pharmacogenomics and drug development. Am Health Drug Benefits. 2010. 3 (2): 79-80.
[5] Grembowski D, Schaefer J, Johnson KE, Fischer H, Moore SL, Tai-Seale M, Ricciardi R, Fraser JR, Miller D, LeRoy L; AHRQ MCC Research Network. A conceptual model of the role of complexity in the care of patients with multiple chronic conditions. Med Care. 2014 Mar;52 Suppl 3:S7-S14.








Leave A Comment